糖鎖の生命分子構造学
糖鎖は、タンパク質や脂質と結びつき、発生・分化・免疫・神経活動といった様々な生命現象にとって重要な役割を果たしています。また、インフルエンザウイルスの感染やがんの浸潤・転移などには、細胞表面の糖鎖構造が密接に関わることが知られており、医療や創薬の分野での注目も高まっています。しかし、糖鎖を対象とした構造生物学研究は、なかなか進んでいません。糖鎖の情報はタンパク質のようにゲノムに直接コードされておらず、糖鎖の発現制御や構造解析が困難なことが主な理由です。私たちの研究室では、生化学や分子生物学、遺伝子工学の手法に加えて、有機合成化学・超分子化学・計算機シミュレーションなどを積極的に応用し、糖鎖の立体構造から分子間相互作用に至るまでを解析する方法論を開発しています。この取組みによって、複雑な枝分かれ構造を持った糖鎖がダイナミックに揺れ動く様子を描象することにも成功しています。私たちはこうした研究成果を通して、糖鎖が担う生命情報を解読することを目指しています。
- 主要な原著論文および総説
- Kato, K. et al. (2022) Trends Glycosci. Glycotech.34, E85-E90.
- Watanabe, T. et al. (2021) Phys. Chem. Chem. Phys. 23, 9753-9760.
- 谷中冴子ら(2023) 化学, 75, 30-71 (2020)
バイオ医薬品の高機能化に向けて
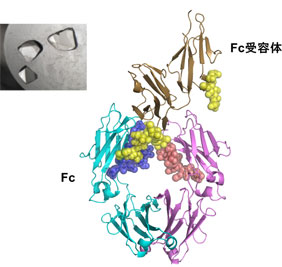
抗体のFcとその受容体の複合体の単結晶と3次元構造。ボールモデルで示したのが糖鎖。
抗体は免疫システムにおける主要な糖タンパク質です。抗体は現在臨床の現場で用いられているバイオ医薬品の中核を占め、分子標的薬としての地位を確立しつつあります。抗体のFc領域には糖鎖が結合しており、健常人では発現している糖鎖の種類と割合はおおむね一定しています。私たちはこれまでに、生理的条件の変化や病態に依存して、抗体の糖鎖の発現パターンが際立って変動することを明らかにしてきました。また、構造生物学的アプローチによって抗体の糖鎖からフコース残基を取り除くことに伴ってナチュラルキラー細胞を介した抗体依存性細胞障害活性が劇的に向上するメカニズムも明らかにしています。このような知見に基づく糖鎖のエンジニアリングは、バイオ医薬品の高機能化の有効な戦略として利用できるものと期待されています。
- 主要な原著論文および総説
- Yanaka, S. et al. (2023) Front. Immunol. 14, 1090898.
- 谷中冴子ら (2023) 生物工学会誌, 101, 347-349.
- 加藤晃一ら (2022) 実験医学, 40, 3253-3258.
先天性筋ジストロフィーの発症にかかわる糖鎖の構造機能解析
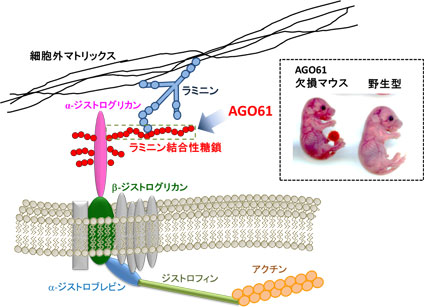
αジストログリカン上の糖鎖は基底膜と細胞膜をつなぎとめることにより細胞骨格を維持しています。この糖鎖の発現異常により、先天性筋ジストロフィーが引き起こされます。
先天性筋ジストロフィーの患者には、細胞膜上に存在するタンパク質であるα-ジストログリカン(αDG)上の糖鎖の発現異常が認められています。αDG上の糖鎖は、ラミニンなどの細胞外に存在するタンパク質との相互作用を通じて細胞の基底膜と細胞膜をつなぎとめています。特に、神経系においては、神経細胞の移動に関与しており、脳形成において重要な役割を担っています。このようにαDG上の糖鎖は非常に重要な機能を担っているにも関わらず、未だその全体構造は明らかとなっていません。私たちは先天性筋ジストロフィーの原因遺伝子の1つであるAGO61が欠損したマウスを作成し、生体内におけるAGO61の機能を明らかにしています。こうしたアプローチによって難治性疾患である先天性筋ジストロフィーの新たな治療法の開発に寄与したいと考えています。
- 主要な原著論文および総説
- Umezawa, F. et al. (2022) Int. J. Mol. Sci. 23, 6662.
- Yamasaki, F. et al. (2021) Biochem. Biophys. Res. Commun. 579, 8-14.
アルツハイマー病の解明と治療薬開発を目指して
アルツハイマー病やプリオン病といった神経変性疾患の発症には、神経細胞膜上でクラスターを形成している糖脂質の存在が深く関わっています。特に、神経系に豊富に存在する糖脂質であるGM1ガングリオシドが、アルツハイマー病に関わる、アミロイドβというアミノ酸約40個が連結したタンパク質の異常会合を引き起こすことが注目されています。しかしながら、その詳細な分子メカニズムは明らかとはなっていません。私たちは、超高磁場NMR装置を用いてアミロイドβとGM1ガングリオシドの相互作用の構造的基盤を明らかにすることに取り組んできました。その結果から、アミロイドβは中央部分にαへリックス構造を形成してGM1ガングリオシドクラスター上に横たわるかたちで結合していることが明らかとなりました。このような構造情報に基づいた創薬への展開が熱い注目を集めています。さらに、宇宙の微小重力条件を利用して、アミロイド形成プロセスを制御することなどを試みています。
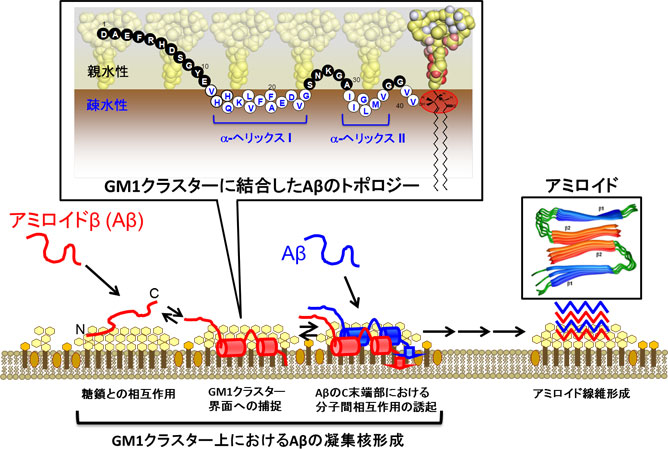
GM1クラスター上におけるAβの凝集核形成機構。ガングリオシドクラスターは、Aβの特異的な結合・構造変化・アミロイド線維形成を促す舞台となり、アルツハイマー病の発症に関与しています。
- 主要な原著論文および総説
- Yagi-Utsumi, M. et al. (2023) ACS Chem. Neurosci. 14, 2648-2657.
- 矢木真穂ら (2021) 膜, 46, 2-6.
- Yagi-Utsumi, M. et al. (2021) NPJ Microgravity, 6, 17.
糖鎖はタンパク質の細胞内での運命を決める
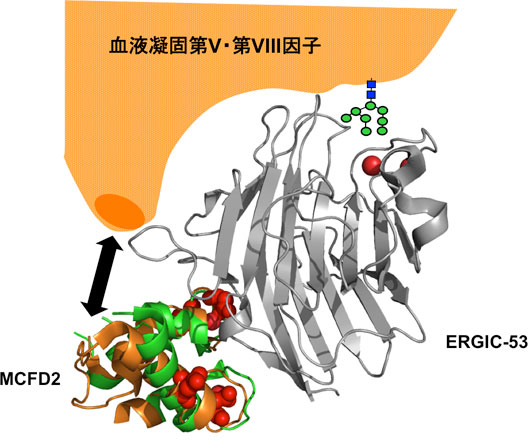
血液凝固因子の細胞内輸送を担う受容体タンパク質ERGIC-53とMCFD2の相互作用。
糖鎖はタンパク質の細胞内の運命を決めています。分泌経路の入り口である小胞体でシャペロンは糖鎖を認識してタンパク質の立体構造を整えています。立体構造形成に失敗したタンパク質を選別し、再生もしくは破壊するための緻密な品質管理の目印になっているのも糖鎖です。この小胞体品質管理システムが破綻すると、不要なタンパク質が細胞内に蓄積して細胞の機能不全や細胞死をもたらし、様々な疾患を引き起こします。私たちは、タンパク質の細胞内品質管理システムが働く仕組みに着目しています。例えば、血液凝固因子の細胞内輸送を司る受容体タンパク質の立体構造を明らかにすることに成功しました。こうした研究を通じて、品質管理システムの破綻に伴う疾患の発症メカニズムの解明や創薬への応用を目指した研究を進めています。
- 主要な原著論文および総説
- Saito, T. et al. (2022) Commun. Biol. 5, 676.
- Yagi, H. et al. (2020) Nature Commun. 11, Article number: 1368.
- 矢木宏和ら (2021) バイオサイエンスとバイオインダストリー, 79, 472-476.
細胞内のタンパク質分解装置プロテアソームの立体構造形成メカニズムの解明

巨大なタンパク質分解装置プロテアソームの分子集合の謎を解く。
プロテアソームはライフサイエンス史上最も巨大で複雑な超分子複合体であり、ユビキチンを介した選択的なタンパク質の分解を行うことによって、細胞周期・免疫応答・シグナル伝達・転写制御・DNA 修復など生命現象の諸相で重要な役割を果たしています。また、プロテアソーム阻害剤は様々ながんの治療薬として注目されています。高齢化社会を迎えた今日、ユビキチン-プロテアソームシステムの破綻に伴って発症する疾患(アルツハイマー病やパーキンソン病などの神経変性疾患)が急増しています。私たちはプロテアソームが形成される仕組みに着目して標的とする創薬を目指した構造生物学研究を行っています。
- 主要な原著論文および総説
- Song, C. et al. (2021) Int. J. Mol. Sci. 22, 4519.
- Sekiguchi, T. et al. (2019) Int. J. Mol. Sci. 20, 2308.
生体分子の構造・動態・機能の解析から生命の環境適応の仕組みに迫る
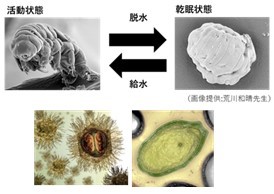
クマムシ(上)や巨大ウィルス(下)に着目し、生命の環境適応の仕組みを理解する。
深海などの極限環境で活動する生命体は、生態環境に適合するための独自の分子機構を備えているものと考えられます。一方、私達の身近な環境においても、外的条件の極端な変動に適応するために、乾眠にみられるようなユニークな適応戦略を備えた生命体が存在しています。私たちは生命活動を司る分子集団の構造・動態・機能の解析を通じて生命の環境適応の仕組みを理解することを目指しています。得られた知見に基づいて、新たな機能の創成に向けた生物工学的な応用研究の展開も目指しています。
- 主要な原著論文および総説
- 矢木真穂ら (2022) 生化学 94, 888-891.
- 矢木真穂ら (2022) 生物物理 62, 232-234.
- Yagi‐Utsumi, M. et al. (2021) Sci. Rep. 11, 21328.
